Stem Cell Res Ther|生育力保持教育部重点实验室付旭锋/裴秀英:人脐带MSC源外泌体通过SMURF1介导的卵巢颗粒细胞铁死亡抑制减轻化疗诱导的卵巢功能不全
卵巢功能不全(POI)是一种40岁以下的女性卵巢功能过早下降为特征的临床综合征,影响全球约1%-5%的育龄妇女并与不孕症密切相关。目前POI的临床治疗主要是通过激素替代疗法来维持月经,缓解雌激素缺乏引起的相关症状。然而,由于相关治疗的副作用和卵巢功能衰竭的不可逆性导致其长期应用受到限制,因此迫切需要新的治疗方法。间充质干细胞外泌体(MSC-Exos)是由间充质干细胞分泌的具有双层脂质膜的细胞外囊泡,携带了多种蛋白质、脂质和非编码RNA等,具有较好的临床应用潜能。MSC- exos不仅有MSCs的生物学特性,而且具有更高的稳定性、生物相容性和更低的免疫排斥风险,同时也规避了移植后生存率低和引起栓塞的风险。因此,MSC- exos治疗成为再生医学中有前景的无细胞应用策略。虽然已有研究表明人脐带间充质干细胞的外泌体(HucMSC-Exos)可以有效地恢复卵巢功能,但具体机制尚不完全清楚。
近日,宁夏医科大学生育力保持教育部重点实验室付旭锋/裴秀英团队在Stem Cell Research & Therapy杂志上发表题为“HucMSC-derived exosomes alleviate chemotherapy-induced premature ovarian insufficiency via SMURF1-mediated inhibition of ferroptosis in ovarian granulosa cells”的研究论文。主要介绍了HucMSC-Exo通过将SMURF1传递给卵巢颗粒细胞,促进了HO-1的泛素化降解并减少了Fe2+的积累,从而减轻颗粒细胞铁死亡并改善了化疗诱导的卵巢损伤。生育力保持教育部重点实验室付旭锋和裴秀英教授为论文共同通讯作者,青年教师许博和韩杭老师为文章共同第一作者。

在该研究中,作者分离了人脐带间充质干细胞的外泌体(HucMSC-Exos)并进行了表征。随后将HucMSC-Exos移植到环磷酰胺(CTX)诱导的卵巢功能不全小鼠模型,发现HucMSC-Exo不仅能够显著改善卵巢功能并减少卵泡闭锁,而且能够调控铁离子的异常积累和脂质过氧化减轻卵巢颗粒细胞的铁死亡。
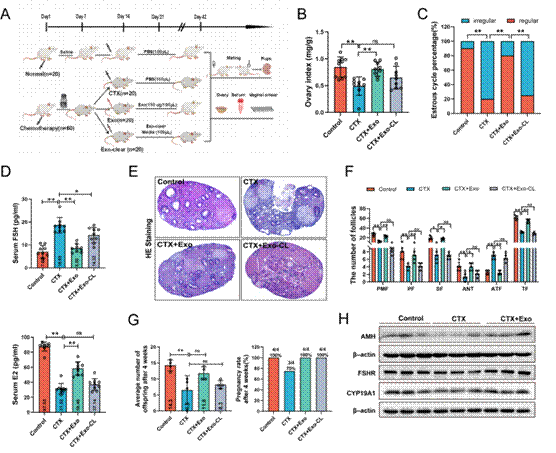
图1. HucMSC-Exos改善POI模型的卵巢功能
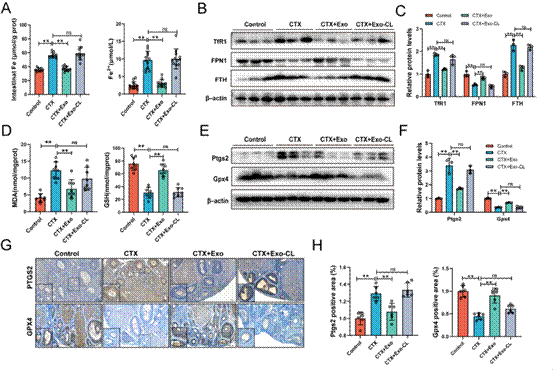
图2. HucMSC-Exos减轻卵巢颗粒细胞中的铁过载和铁死亡
值得注意的是,研究进一步发现HucMSC-Exos中存在SMURF1的E3泛素连接酶并将其递送到卵巢颗粒细胞后促进铁代谢关键调控蛋白HO-1的泛素化降解,进而减轻亚铁离子的积累和脂质过氧化进程,最终通过降低卵巢颗粒细胞的铁死亡改善卵巢功能。
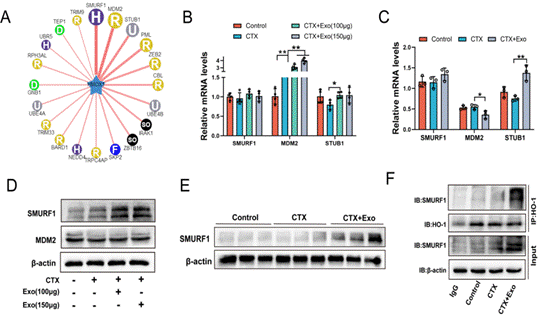
图3. HucMSC-Exos传递SMURF1到颗粒细胞并促进HO-1泛素降解
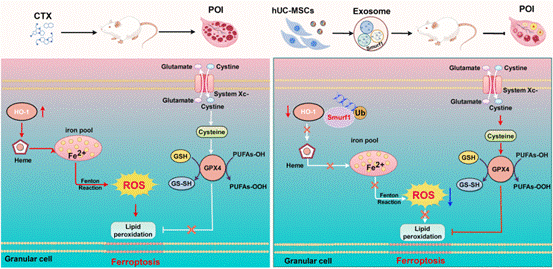
图4:HucMSC-Exos减轻卵巢颗粒细胞铁死亡的机制
该研究揭示HucMSC-Exos通过SMURF1/HO-1途径调控卵巢颗粒细胞铁死亡进而改善化疗所致的卵巢功能损伤,为POI的治疗提供了新思路。这一发现不仅深化了对干细胞外泌体修复机制的理解,也为开发无细胞、低免疫原性的生物疗法奠定了理论基础。
参考文献:
HucMSC-derived exosomes alleviate chemotherapy-induced premature ovarian insufficiency via SMURF1-mediated inhibition of ferroptosis in ovarian granulosa cells. Stem Cell Res Ther. Published online January 8, 2026. doi:10.1186/s13287-026-04893-x
